传统标准漏诊76%高危患者?MRD引领膀胱癌术后精准免疫新时代
新闻来源: 发布时间:[2026-02-11]
概述
膀胱癌每年新增病例超过57万例,其中约25%为肌肉侵袭性疾病(MIBC)。符合顺铂条件患者的标准治疗是新辅助化疗(NAC)后进行根治性膀胱切除术(RC)。尽管如此,近一半的病例在两年内复发当前的风险评估未能可靠识别最高风险者。目前,辅助免疫疗法已被证明能改善高风险患者的无病生存率[1]。
因此,欧洲药品管理局批准将辅助免疫疗法用于高危PD-L1阳性患者。病理和临床评估的变异性以及PD-L1表达预测准确性有限,增加了过度或不足治疗的风险。这凸显了可靠的生物标志物以检测微残病(MRD)、指导辅助治疗并实现及时干预的必要性。此类生物标志物还可能支持低风险患者的治疗降级,降低毒性并优化医疗资源的利用[2]。
TOMBOLA是一项丹麦的多中心、开放标签、单臂II期临床试验,评估用于指导术后免疫治疗的循环肿瘤DNA(ctDNA)检测。采用NAC和RC治疗的低危和高风险MIBC(cT2–4aN0–1M0)患者,术后通过肿瘤知情的ctDNA检测进行监测。ctDNA阳性(ctDNA+)患者无论影像如何,均开始使用阿替唑珠单抗最长1年;ctDNA阴性(ctDNA–)患者仅在X线检测转移后接受免疫治疗。主要终点为在ctDNA阳性时启动免疫治疗的完全反应(CR),无论是否CT检测到转移。CR定义为治疗期间最后可用血浆样本的ctDNA清除率,且影像上无疾病。
次要终点包括无复发生存期(RFS;从RC到放射复发或死亡)、生化复发患者的RC后总体生存期(OS)、按生物标志物分层的免疫疗法反应、治疗期间ctDNA水平下降或稳定患者的临床无复发生存期,以及NAC反应(病理性降级至T0或<T2)及其与ctDNA的相关性。
共计192名患者,在意向治疗人群中178名可评估患者(中位随访34个月),其中104人(58%)在RC后2年内完成ctDNA+,63%在4个月内完成。从ctDNA检测到影像确认复发的中位时间为90天(范围为-61至961天)。在ctDNA+患者中,84人完成了阿替唑珠单抗治疗,并有扫描和ctDNA分析可供主要终点评估。60%的患者(50/84%)达到了完全缓解的主要终点。ctDNA患者一年无复发生存率为97%,ctDNA+患者为76%。预先指定的生物标志物分析显示,ctDNA状态及水平、风险分层及免疫相关基因表达特征与复发风险及免疫治疗反应均相关。治疗耐受性良好,未出现新的安全隐患。
该研究首次系统评估了利用循环肿瘤DNA(ctDNA)指导肌层浸润性膀胱癌患者在根治性膀胱切除术后进行免疫治疗决策的可行性与有效性,为个体化、精准化术后管理提供了强有力证据。
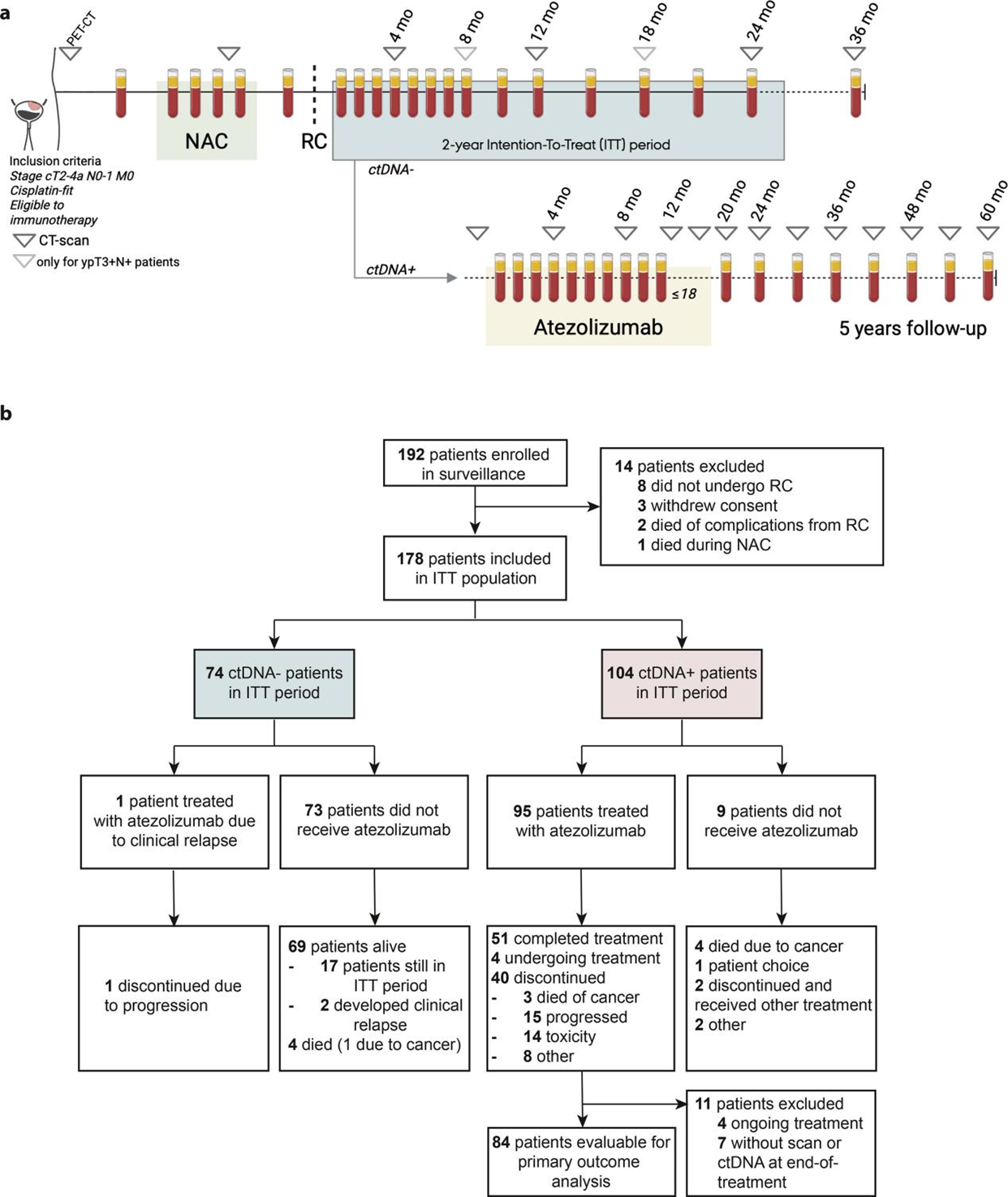
研究设计、方法及患者招募情况
本研究对178名患者术后微小残留病灶(ctDNA)状态与复发风险的关系进行了分析。结果显示,在术后两年随访期内,共有58%的患者检测到ctDNA转为阳性。值得注意的是,在这些ctDNA阳性患者中,依据现有临床病理标准,只有半数的患者被划为传统高风险人群;而同时满足高风险且PD-L1阳性条件的比例仅为24%。这说明,如果单纯依赖当前临床指南进行辅助免疫治疗决策,将有超过四分之三的ctDNA阳性患者失去接受强化治疗的机会。
另一方面,在ctDNA持续阴性的患者群体中,尽管有30%的患者在传统病理分型中被归为高风险类别,但在随访期间,该组患者没有出现任何一例转移性复发事件。这一结果进一步提示,ctDNA在甄别真实复发风险方面具有不可替代的作用。
在治疗干预方面,对84例可评估主要终点的ctDNA阳性患者给予阿替利珠单抗治疗后,有60%实现了分子学与影像学双重完全缓解。分析显示,ctDNA水平的动态变化与影像学复发及无复发生存期密切相关。无论在传统风险分层中的低危或高危亚组,清除ctDNA均预示着更佳的生存结局,这也提示免疫治疗在极低肿瘤负荷状态下依然能够发挥作用。
同时,治疗降级策略在ctDNA阴性患者中也显示出良好的安全性。术后一年随访数据显示,该组患者的无复发生存率达97%,总生存率达到100%。这证实,即便患者符合传统高风险病理特征,只要ctDNA持续阴性,免于辅助免疫治疗并不影响其良好预后,从而有效避免了不必要的过度治疗[3]。
TOMBOLA试验公布了首批成果,中位随访期为34个月。数据显示,根据肿瘤知情液体活检结果对ctDNA阴性患者实施治疗降级策略是安全的——术后一年无复发生存率(RFS)达到97%。该结果提示,当前临床指南可能导致部分患者接受过度治疗,因为无论是否给予辅助免疫治疗,ctDNA阴性患者的预后均未受影响。
而在ctDNA阳性患者中,使用阿替利珠单抗治疗一年后的RFS为75%,且无论传统风险分层如何(高风险与低风险组),均观察到疗效。治疗期间ctDNA清除率达到60%,该比例显著高于以往仅基于影像学评估的免疫治疗研究中所报告的反应率。这一差异很可能源于ctDNA作为一种分子标志物,比放射学评估能更早、更灵敏地反映治疗反应。
综上所述,TOMBOLA试验表明,ctDNA阳性患者(包括传统低风险人群)可受益于早期免疫治疗;而对于ctDNA阴性患者,即使符合传统高风险标准,也可安全豁免辅助治疗,且不影响预后。这种以生物标志物为导向的个体化策略,有望在保障疗效的同时减少过度治疗,提升患者生活质量,并促进医疗资源的合理利用。
声明:本文仅用于分享,如涉及版权等问题,请尽快联系我们,我们第一时间更正,谢谢!