子宫内膜癌各分子亚型的特征和临床意义
新闻来源: 发布时间:[2022-04-11]
前言
众所周知,采用分子检测的方法,子宫内膜癌被分为四组具有较为显著的预后差异的分子亚型。NCCN指南参考TCGA的命名方式,即POLE突变型、MSI-H型、高拷贝数型和低拷贝数型[1]。WHO结合了多种分型方法的命名,分为POLE突变型(POLE mut)、MMRd型、p53异常型(p53 abn)和无特异分子谱组(NSMP)[2]。国内专家共识推荐与WHO保持一致[2]。分子分型的检测方法包括NGS(全分型),免疫组化(MMR蛋白、p53蛋白),Sanger测序(POLE热点突变)和片段分析(MSI)等。无论采用任何一种检测或命名方法,四个亚型基本上呈一一对应关系。在这里我们进行一项简单的工作,总结和归纳各亚型的特征和临床意义。
POLE突变型
01
占比
7%(TCGA)、9.3%(ProMisE)、12.4%(PORTEC-3)[3-5]
02
分子特征[2-3][6-7]
几乎没有拷贝数改变。
突变频率非常高(232个突变/Mb)。
常见突变基因:POLE(100%)、PTEN(94%)、FBXW7(82%)、PIK3CA(71%)、PIK3R1(65%)、KRAS(53%)、FGFR2(29%)。
基因表达变化:ASNS和CCNB1表达上升。
其他特征:C→A颠换频率增加。
大多数为MSS。
PIK3CA与PIK3R1在除POLE突变型以外的亚型中互斥。
POLE和POLD1有报道过胚系易感性变异,但发生率仅有0.1%~0.4%。
热点突变包括P286R、V411L、S297F、A456P和S459F,另有6个位点通过突变评分系统判定为致病突变。
03
临床特征[4]
预后较好
中位年龄58.8岁(各亚组最低)
BMI:27.1(各亚组最低)
FIGO II期以上肿瘤:7.1%
G3肿瘤:14.3%
非内膜样癌:9.5%
LVSI:11.9%
深肌层浸润:21.4%
淋巴结阳性:0%
ESMO风险分类高危型患者:16.7%
04
临床意义
1.POLE突变是子宫内膜癌预后良好的标志;即便是在传统认为预后较差的高级别肿瘤中,POLE突变型0复发[8]。
2. I~II期POLE突变的内膜样癌,术后不推荐进行辅助治疗;但III期以上的POLE突变的内膜样癌,其预后还缺乏证据[9]。
3. ProMisE研究提示,POLE突变型肿瘤淋巴结0转移,手术时可考虑不切除淋巴结[4]。
4.POLE突变型的肿瘤浸润淋巴细胞较多,PD-1过表达,肿瘤局部微环境中免疫应答反应活跃,新生抗原水平高,提示免疫治疗获益[10-12]。
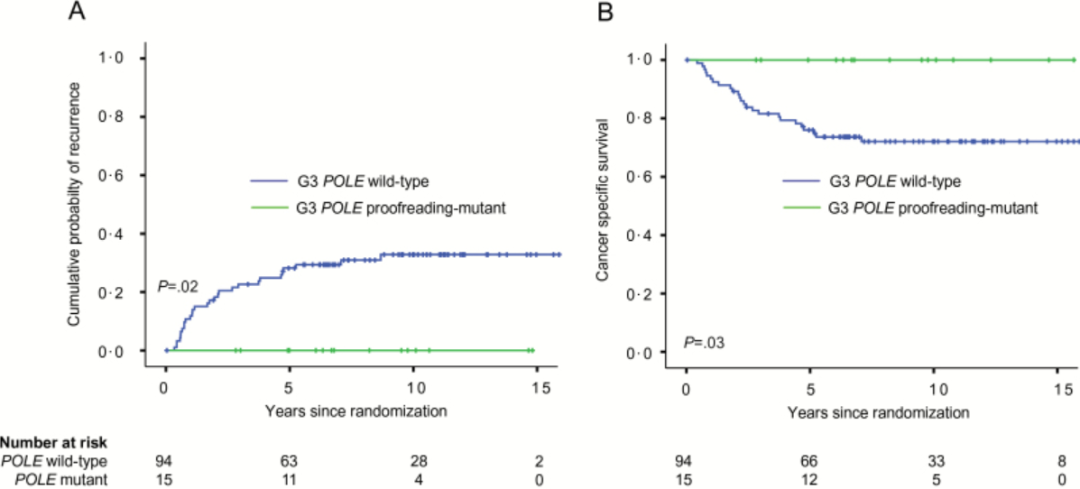
▲POLE突变型预后良好,即便是G3肿瘤[8]
MSI-H型/MMRd型

▲dMMR/MSI-H是免疫治疗疗效重要的分子标志物[1]
01
占比
28%(TCGA)、28.1(ProMisE)、33.4%(PORTEC-3)[3-5]
02
分子特征[3][6]
较少的拷贝数改变。
突变频率高(18个突变/Mb)。
常见突变基因:PTEN(89%)、PIK3CA(54%)、PIK3R1(40%)、ARID1A(37%)、RPL22(37%,主要为移码缺失)、KRAS(35%,主要为非同义突变)、ARID5B(23%)。
基因表达变化:部分MLH1 mRNA表达降低;AKT磷酸化水平上升。
其他特征:MSI-H;大部分具有MLH1启动子甲基化。
03
临床特征[4]
预后中等
中位年龄67.7岁
FIGO II期以上肿瘤:22%
G3肿瘤:19.7%
非内膜样癌:7.1%
LVSI:20%
深肌层浸润:45.7%
淋巴结阳性:9.4%
ESMO风险分类高危型患者:33.9%
04
临床意义
1.PORTEC-3研究提示,MMRd型患者术后化疗无获益[5]。
2.dMMR/MSI-H是帕博利珠单抗、纳武利尤单抗、Dostarlimab和Avelumab等ICI药物在子宫内膜癌患者治疗时的伴随诊断或补充诊断[1]。
3. dMMR/MSI-H是林奇综合征筛查的分子标志物[2]。
4.一项韩国的小规模研究显示,I期MMRd型患者对激素治疗不敏感,且有数例因治疗失败而立即进行子宫切除[13]。
5. MLH1甲基化的患者预后较差,免疫治疗疗效明显劣于MMR基因突变的患者[14]。
高拷贝数型/p53异常型
01
占比
26%(TCGA)、12.2%(ProMisE)、22.7%(PORTEC-3)[3-5]
02
分子特征[3][6]
较多拷贝数改变。
常见扩增基因:HER2(25%)、MYC、CCNE1、FGFR1、FGFR3、SOX17、LRP1B(缺失)。
突变频率低(2.3个突变/Mb)。
常见突变基因:TP53(92%)、PIK3CA(47~60%)、FBXW7(22%)、PPP2R1A(22%)、PTEN(11~15%)、ARID1A。
基因表达变化:细胞周期失调相关基因(CCNE1、PIK3CA、MYC、CDKN2A)和TP53表现出最大转录活性;PTEN和ARID1A表达在p53异常型以外的亚型中降低;AKT磷酸化水平降低。
信号通路:MYC/MAX信号相对较高,ER/FOXA1信号较低。
其他特征:甲基化率最低。
约50%的具有TP53突变的高级别内膜样癌中存在PTEN突变,此时TP53和PTEN均为非沉默突变;浆液性癌中鲜见PTEN基因突变(2%)。
TP53截断突变与功能缺失有关,表明不同类别的p53突变具有不同的蛋白表达。
03
临床特征[4]
预后较差
中位年龄71.7岁(各亚组最高)
FIGO II期以上肿瘤:47.3%
G3肿瘤:85.5%
非内膜样癌:61.7%(TCGA)、72.7%(ProMisE)
LVSI:28.3%
深肌层浸润:43.6%
淋巴结阳性:34.5%
ESMO风险分类高危型患者:87.3%
04
临床意义
1. p53异常型预后较差,50~70%的子宫内膜癌死亡病例为该亚型患者,需要积极的辅助治疗。低危的IA期内膜样癌如果存在TP53致病突变,将提升为中危[9]。
2.PORTEC-3研究提示,p53异常型患者可以从术后联合放化疗中获益[5]。
3.p53异常型患者中25%存在HER2扩增,可考虑抗HER2疗法[2]。
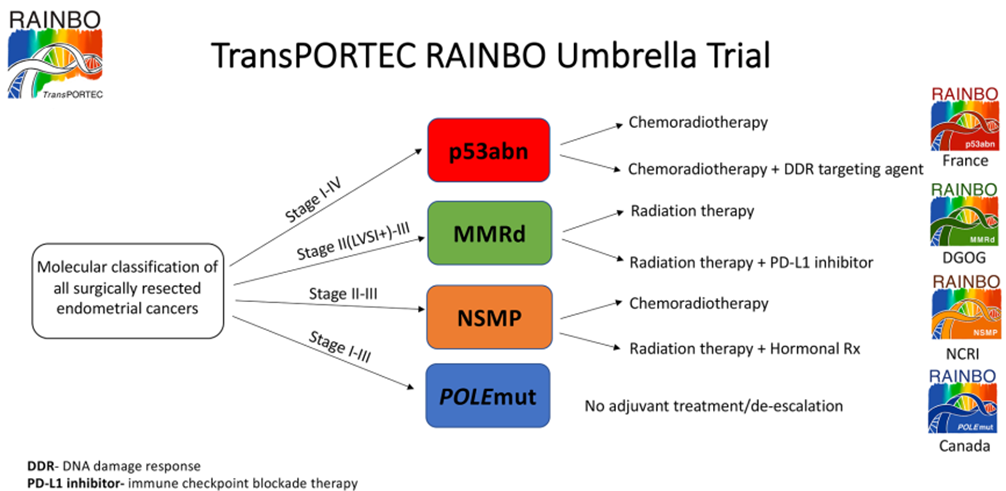
4.p53异常型子宫内膜癌患者与高级别浆液性卵巢癌和基底样乳腺癌之间具有分子机制相似性,约一半的患者存在HRD[3]。RAINBO研究在探索放化疗联合PARP抑制剂的疗法[15]。
— — 仅供科研参考使用 — —