如何评价肿瘤病情的进展、稳定or缓解?
新闻来源: 发布时间:[2023-05-05]
背景
RECIST(The Response Evaluation Criteria In Solid Tumors)标准是一系列肿瘤治疗效果的定义,即有效、稳定、无效。该指南主要介绍实体瘤测量和成人、小儿癌症的临床试验中肿瘤大小变化客观评估的规定的标准方法。1981年WHO首次出版了肿瘤反应标准,2000年EORTC、NCI、NCIC制定了新的标准RECIST1.0版,2009年进行了修订为RECIST1.1版。

图一
肿瘤疗效评价按照RECIST 1.1[1]分为四个等级:完全缓解(CR),部分缓解(PR),疾病稳定(SD),疾病进展(PD)。肿瘤疾病部位评价必须采用与基线相同的方法,包括一致进行增强和及时的扫描。
具体评价步骤为:
1.基线期记录目标病灶和非目标病灶;
2.按照标准对目标病灶和非目标病灶进行评价;
3.综合进行总体评价。
肿瘤病灶基线记录
靶病灶:所有累及器官达最多2个病灶/每个器官,共5个病灶,所有可测量病灶应视为基线目标病灶。
非靶病灶 :所有不可测量的疾病均为非目标病灶病灶。所有未鉴别为目标病灶的可测量病灶也纳入非病灶疾病。
01可测量病灶
肿瘤病变至少有一条可以精确测量的径线的病灶,最长径待记录。
1)根据CT或MRI评价,病灶最长直径至少为10 mm(2个层厚,层厚不大于5 mm)。
2)根据胸部X线评价,病灶最长直径至少20 mm。
3)根据测径器评价,最长直径≥10 mm的浅表性病灶。
4)恶性淋巴结:病理性增大且可测量,单个淋巴结CT扫描短径须≥15 mm(CT扫描层厚推荐不超过5 mm)。基线和随访中,仅测量和随访短径。
注:恶性肿瘤淋巴结用最短轴作为直径,其它可测量病灶用最长轴。
02不可测量病灶
所有其他病变,包括小病变(直径最长<10mm或P10至<15mm的病理性淋巴结短轴)以及真正不可测量的病变。病变被认为真正不可测量的疾病包括:
1)软脑膜疾病;
2)腹水、胸腔或心包积液;
3)炎症乳腺疾病、皮肤或肺部淋巴管受累;
4)腹部肿块/腹部器官肿大,无法通过可重复成像测量的体检技术。
注:许多学者认为,在患者接受治疗后,尽管从影像学上似乎彻底清除了病灶,但仍有极少量未被检测到的肿瘤细胞残存或肿瘤细胞来源分子异常[2]。这些残存的肿瘤病灶被称之为微小残存病灶(MinimalResidual Disease,MRD),也可称之为分子残存病灶(Molecular Residual Disease)。MRD作为影像学层面“不可测量病灶”也受到越来越多的关注与研究。
03其他特殊情况
1)骨病变:骨骼扫描、PET扫描或平片被认为不能够作为测量骨骼病变的成像技术。然而,这些技术可以用来确认骨骼病变的存在或消失。
2)既往局部治疗:既往放疗病灶(或其它局部治疗的病灶)为不可测量病灶,除非治疗完成后进展。
3)正常部位:单纯囊肿不应被视为恶性病变(既不可测量也不应被记录为目标病灶);正常结节:短轴<10 mm的结节被视为正常,不应记录或安装可测量或不可测量病灶分类。
靶病灶的评估
CR(完全缓解):所有靶病变消失。任何病理性淋巴结(无论是靶淋巴结还是非目标)必须在短径上缩小到<10毫米。
PR(部分缓解):靶病灶直径之和比基线水平减少至少30%。
SD(疾病稳定):靶病灶减小的程度没达到PR,增加的程度也没达到PD水平,介于两者之间,研究时可以直径之和的最小值作为参考。
PD(疾病进展):总数至少增加20%目标病变的直径,作为参考研究中的最小总和(包括基线如果这是研究中最小的总和)。除了20%的相对增长,总和也必须证明绝对增加至少5毫米。(注:一个或多个新病变的出现也是考虑的进展)。
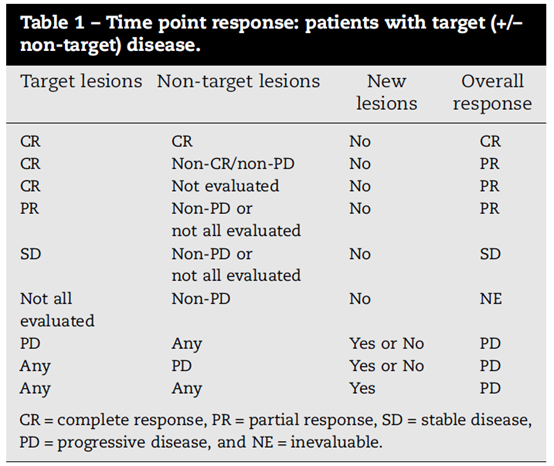
图二
非靶病灶的评估
CR(完全缓解):所有非靶病灶消失或肿瘤标志物水平正常。所有淋巴结大小必须正常(短轴<10 mm)。
非PR/非PD:任何非目标病灶持续存在和/肿瘤标志物水平高于正常上限。
PD(疾病进展):靶病灶为PR/SD时,罕见非靶病灶的明确增大而评价进展。(注:一个或多个新病变的出现也应考虑进展)。
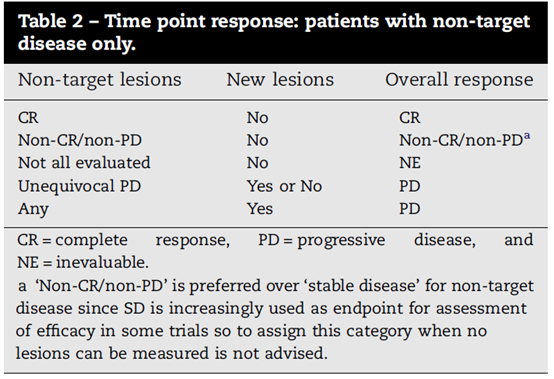
图三
新病灶
出现任何新发明确的恶性肿瘤病灶都表明PD。如果新病灶不明确,或由于体积较小无法测量,应持续保持重复扫描评价,如果重复评价明确为新病灶,那么应在首次评价日期记录进展PD。在以前未扫描区发现的病灶被认为是新病灶。
小提示
综上内容,就靶病灶的评估,评价PR不仅仅是靶病灶的缩小,需满足缩小达到30%,同理评价PD也不仅仅只是靶病灶的增大,需满足病灶增大20%和增大超过5mm。然而整体的评价,还有参考非靶病灶、新病灶等诸多信息,专业的评估还是以临床医生的意见为准!
参考文献
[1].New response evaluation criteria in solid tumours: Revised RECIST guideline (version 1.1)
[2].Nat Rev Clin Oncol, 2017, 14(6): 325-326.
声明:本文仅用于分享,不代表平台立场,如涉及版权等问题,请尽快联系我们,我们第一时间更正,谢谢!